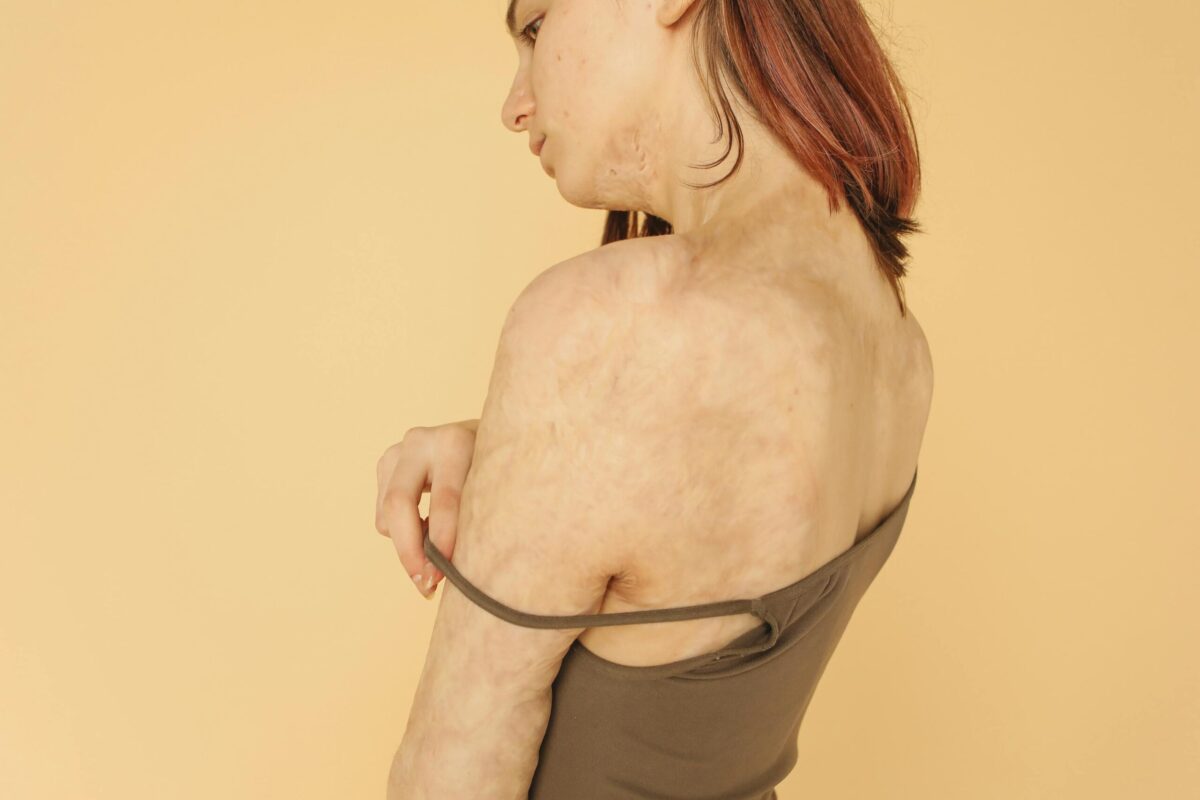
Toczeń rumieniowaty to ciężka choroba autoimmunologiczna, która może prowadzić do powstawania trwałych blizn oraz zmian skórnych. Podczas dorocznego Kongresu Amerykańskiej Akademii Dermatologii ogłoszono wyniki nowego badania, które dają nadzieję na skuteczniejsze leczenie.
Toczeń rumieniowaty – dla tych pacjentów brakuje celowanej opcji leczenia
Firma Biogen Inc. (Nasdaq: BIIB) ogłosiła pozytywne wyniki badania Fazy 2 prowadzonej w ramach badania AMETHYST (Część A) dotyczącej stosowania litifilimabu u osób ze skórną postacią tocznia rumieniowatego (Cutaneous Lupus Erythematosus, CLE). Litifilimab to humanizowane przeciwciało monoklonalne klasy IgG1 (mAb) ukierunkowane na antygen 2 komórek dendrytycznych krwi (BDCA2), które ma potencjał stać się pierwszą innowacyjną terapią dopuszczoną do obrotu w leczeniu CLE po raz pierwszy od 70 lat. W części A badania AMETHYST oceniano skuteczność i bezpieczeństwo litifilimabu do tygodnia 24., odnotowując spadek aktywności zmian skórnych w oparciu o szereg różnych wskaźników. Wyniki pozostają spójne z pozytywnymi rezultatami uzyskanymi we wcześniejszym badaniu fazy 2 LILAC, opublikowanymi w czasopiśmie The New England Journal of Medicine.
– „Dysponujemy dzisiaj spójnymi wynikami z badań fazy 2 nad litifilimabem, które pokazują istotny spadek aktywności zmian skórnych w CLE. To ważny moment w tym programie badań. Rezultaty są bardzo obiecujące i wspierają potencjał wprowadzenia litifilimabu dla pacjentów ze skórną postacią tocznia rumieniowatego – chorobą, dla której w chwili obecnej brak jest dopuszczonych do obrotu terapii celowanych oraz istnieją istotne niezaspokojone potrzeby medyczne” – powiedział dr n. med. Joseph F. Merola, Profesor i Kierownik Kliniki Dermatologii oraz Profesor Chorób Wewnętrznych w Ośrodku Chorób Reumatycznych Południowo-Zachodniego Centrum Medycznego Uniwersytetu Teksańskiego (UT Southwestern Medical Center). – „Te ustalenia, wraz z przyznaniem przez FDA statusu terapii przełomowej, pokazują potencjał, jaki w przypadku dopuszczenia do obrotu, może dawać litifilimab pacjentom żyjącym z tą niełatwą chorobą. Oprócz wyników dotyczących skuteczności, litifilimab wykazał również profil bezpieczeństwa zgodny z rezultatami wcześniejszych badań. Co istotne, do badania celowo włączono populację reprezentatywną w skali globalnej, odzwierciedlającą zróżnicowane postaci CLE, w tym liczną grupę pacjentów z umiarkowaną lub ciężką postacią choroby w chwili rozpoczęcia badania”.
Badanie AMETHYST – co warto o nim wiedzieć?
Skórna postać tocznia rumieniowatego (CLE) to choroba o złożonym i heterogennym przebiegu, dotykająca miliony osób na całym świecie. W chwili obecnej brak jest terapii celowanych zatwierdzonych do jej leczenia.
AMETHYST to trwające, sekwencyjne, dwuetapowe, wieloośrodkowe, podwójnie zaślepione, randomizowane i kontrolowane placebo badanie, oceniające skuteczność i bezpieczeństwo litifilimabu w porównaniu z placebo u uczestników z CLE o różnym stopniu nasilenia. Uczestnicy są losowo przydzielani do grupy otrzymującej podskórnie litifilimab w połączeniu ze standardowym postępowaniem leczniczym (SoC) lub placebo podawane co cztery tygodnie w skojarzeniu z SoC. Wszyscy uczestnicy będą otrzymywali litifilimab w trakcie 28-tygodniowego wydłużonego okresu leczenia, od tygodnia 24. do tygodnia 48. Ogłaszane wyniki pochodzą z podwójnie zaślepionego, kontrolowanego placebo badania fazy 2 AMETHYST (Część A), obejmującej okres od 0. do 24. tygodnia. Kobiety stanowiły 74% uczestników badania, a 33% uczestników reprezentowało populacje inne niż biała. Taki rozkład demograficzny pozostaje spójny z epidemiologią CLE – chorobą, która zdecydowanie częściej występuje u kobiet oraz w grupach zróżnicowanych etnicznie i rasowo. Faza 3 badania nadal trwa, a wyniki pozostają zanonimizowane.
Co wykazało badanie AMETHYST?
W części A badania AMETHYST osiągnięto pierwszorzędowy punkt końcowy, wykazując, że litifilimab powodował statystycznie istotne, tj. o 11,8% większe, zmniejszenie aktywności choroby u osób z CLE (95-procentowy przedział ufności [CI]: 1,39–22,27; p < 0,05), mierzonej wynikiem 0–1 dla rumienia (brak/niemal całkowity brak) w Zrewidowanej Globalnej Skali Oceny Aktywności skórnej postaci tocznia rumieniowategonwg Badaczy (Cutaneous Lupus Activity Investigators’ Global Assessment Revised, CLA-IGA-R) w tygodniu 16., w porównaniu z placebo (14,7% w stosunku do 2,9%). Ponieważ w części A drugorzędowych punktów końcowych, w tym wymienionych poniżej, nie skorygowano pod kątem wielokrotności, nie można formalnie wykazać ich istotności statystycznej. Niemniej jednak stosowanie litifilimabu wiązało się z szybką i utrzymującą się poprawą w aktywności zmian skórnych, z różnicą w stosunku do placebo obserwowaną już w tygodniu 4. (19,3% w stosunku do 5,5%; Δ = 13,8; CI: 1,19, 26,46), mierzoną Wskaźnikiem Obszaru i Stopnia Nasilenia Zmian Skórnych w skórnej postaci tocznia rumieniowatego – CLASI-50 (Cutaneous Lupus Erythematosus Disease Area and Severity Index Activity-50) do tygodnia 24. (40,8% w stosunku do 21%; Δ = 19,8; CI: 1,46, 38,15). Zgodnie z oceną według CLASI-50 przeprowadzoną w tygodniu 24., u większej liczby uczestników otrzymujących litifilimab osiągnięto odpowiedź w porównaniu z grupą placebo. Odpowiedzi CLASI-50 i CLASI-70 określa się jako, odpowiednio, 50- i 70-procentową poprawę w wyniku w CLASI-A w stosunku do wartości wyjściowej. Ponadto, w tygodniu 24., w porównaniu z grupą otrzymującą placebo, co szósty uczestnik przyjmujący litifilimab osiągnął w CLASI wynik 0–3, określany jako brak aktywności choroby lub jej minimalny poziom (16,3% w porównaniu z 0%; różnica = 16,3; CI: 7,07–25,62), podczas gdy w grupie placebo nie odnotowano takich przypadków.
W Części A badania AMETHYST litifilimab był ogólnie dobrze tolerowany, a profil tolerancji był zgodny z profilem bezpieczeństwa ustalonym w zakończonych badaniach, w tym w badaniu 2 fazy LILAC. W okresie 24 tygodni zdarzenia niepożądane (AE) odnotowano u 74,6% (44/59) i 64,7% (22/34) uczestników otrzymujących, odpowiednio, litifilimab i placebo. Większość AE miała nasilenie od łagodnego do umiarkowanego. Poważne zdarzenia niepożądane zgłoszono u 6,8% (4/59) uczestników w grupie litifilimabu i 2,9% (1/34) uczestników w grupie placebo.
– „Skórna postać tocznia rumieniowatego nie tylko pozostawia blizny. Może także wywierać głęboki wpływ na stan emocjonalny i sytuację społeczną osób, które żyją z tą chorobą. Wobec braku zatwierdzonych celowanych terapii modyfikujących przebieg choroby, opcje dostępne dla pacjentów z CLE są mocno ograniczone” – powiedział dr n. med. Daniel Quirk, Globalny Dyrektor Medyczny w firmie Biogen. – „Cieszymy się z wyników dwóch badań, w których litifilimab był dobrze tolerowany a jego stosowanie wiązało się z poprawą zmian skórnych w reprezentatywnej populacji. Dają nam one motywujący impuls do prowadzenia programu badań fazy 3. Prace prowadzone przez firmę Biogen w obszarze tocznia, w tym w szczególności w CLE, to dowód na zaangażowanie firmy w walkę z chorobami, w przypadku których opcje są ograniczone albo ich brak”.
ET/Materiały prasowe
Zobacz także:: Mózg: co mu szkodzi, a co pomaga? Przypominamy w Europejskim Dniu Mózgu